khí đốt lưu huỳnh trong không khí, lưu huỳnh hóa hợp với Oxi thành một chất khí có mùi hắc gọi là khí sunfurơ. Cho biết phân tử khối khí sunfurơ bằng 64 (đvc); biện luận xác định số nguyên tử của từng nguyên tố có trong công thức

Những câu hỏi liên quan
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2. a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí. b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm. -Thể tích khí sunfurơ sinh ra ở đktc. -Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
Đọc tiếp
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2.
a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí.
b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm.
-Thể tích khí sunfurơ sinh ra ở đktc.
-Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
a) Phương trình hóa học S + O2 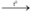 SO2
SO2
b) nS = 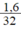 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 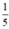 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l
Đúng 1
Bình luận (0)
Lưu huỳnh cháy trong không khí tạo ra khí sunfurơ (SO2) . Đây là một chất khí độc, có mùi hắc, gây ho và là một trong các khí gây ra hiện tượng mưa axit. a) viết phương trình hóa học của phản ứng xảy ra b) tính thể tích khí SO2 tạo ra và thể tích không khí cần dùng để đốt cháy hết 3,2 gam lưu huỳnh ( biết các thể tích khí đo ở đktc; trong không khí oxi chiếm 20% về thể tích.
Đọc tiếp
Lưu huỳnh cháy trong không khí tạo ra khí sunfurơ (SO2) . Đây là một chất khí độc, có mùi hắc, gây ho và là một trong các khí gây ra hiện tượng mưa axit.
a) viết phương trình hóa học của phản ứng xảy ra
b) tính thể tích khí SO2 tạo ra và thể tích không khí cần dùng để đốt cháy hết 3,2 gam lưu huỳnh ( biết các thể tích khí đo ở đktc; trong không khí oxi chiếm 20% về thể tích.
a) PTHH: S + O2 =(nhiệt)=> SO2
b) nS = 3,2 / 32 = 0,1 (mol)
=> nO2 = nSO2 = nS = 0,1 (mol)
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VKK(đktc) = \(2,24\div\frac{1}{5}=11,2\left(l\right)\)
Đúng 0
Bình luận (0)
lưu huỳnh cháy trong không khí tại ra khí sunfurơ (SO2). đây là một chất khí độc, có mùi hắc, gây ho và là một trong các khí gây ra hiện tượng mưa axit.a) viết phương trình hóa học của phản ứng xảy rab) tính thể tích khí SO2 tạo ra và thể tích không khí cần dùng để đốt cháy hết 3,2 gam lưu huỳnh ( biết các thể tích khí đo ở đktc; trong không khí oxi chiếm 20% về thể tích )
Đọc tiếp
lưu huỳnh cháy trong không khí tại ra khí sunfurơ (SO2). đây là một chất khí độc, có mùi hắc, gây ho và là một trong các khí gây ra hiện tượng mưa axit.
a) viết phương trình hóa học của phản ứng xảy ra
b) tính thể tích khí SO2 tạo ra và thể tích không khí cần dùng để đốt cháy hết 3,2 gam lưu huỳnh ( biết các thể tích khí đo ở đktc; trong không khí oxi chiếm 20% về thể tích )
a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia phản ứng :
\(n_S=\frac{3,2}{32}=0,1\left(mol\right)\)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% về thể tích của không khí nên thể tích không khí cần dùng là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
Đúng 0
Bình luận (18)
Lưu huỳnh cháy trong không khí sinh ra khí sunfurơ, theo phản ứng sau:
S + O 2 − t o → S O 2
Hãy cho biết:
Thể tích khí oxi ở đktc cần dùng để đốt cháy hoàn toàn 2,5 mol nguyên tử lưu huỳnh.
lưu huỳnh cháy trong không khí tạo ra khí sunfurơ ( so2) . đây là một chất khí độc , có mùi hắc , gây ho và lầ một trong các khí gây ra hiện tượng mưa axit a) viết phương trình hóa học của phản ứng xảy ra b) tính thể tích khí so2 tạo ra và thể tích không khí cần dùng để đốt cháy hết 3,2 gam lưu huỳnh ( biết các thể tích khí đo ở đktc ; trong không khí õi chiếm 20% về thể tích )
Đọc tiếp
lưu huỳnh cháy trong không khí tạo ra khí sunfurơ ( so2) . đây là một chất khí độc , có mùi hắc , gây ho và lầ một trong các khí gây ra hiện tượng mưa axit
a) viết phương trình hóa học của phản ứng xảy ra
b) tính thể tích khí so2 tạo ra và thể tích không khí cần dùng để đốt cháy hết 3,2 gam lưu huỳnh ( biết các thể tích khí đo ở đktc ; trong không khí õi chiếm 20% về thể tích )
a/ PTHH: S + O2 =(nhiệt)==> SO2
b/ nS = 3,2 / 32 = 0,1 mol
=>nO2 = nSO2 = nS = 0,1 mol
=> VSO2(đktc) = 0,1 x 22,4 = 2,24 lít
=> VO2(đktc) = 0,1 x 22,4 = 2,24 lít
=>Vkhông khí = \(\frac{2,24.100}{20}\) = 11,2 lít
Đúng 0
Bình luận (0)
khi đốt khí lưu huỳnh trong không khí ,lưu huỳnh hoá hợp với õi tạo thành 1 chất khí mùi hắc gọi là khí sunpuro.hỏi khí sunpuro do những ng tố nào tạo nên.là hợp cắt hay đơn chất
\(S+O_2->SO_2\)CHẤT NÀY ĐƯỢC TẠO NÊN TỪ LƯU HUỲNH VÀ OXI, ĐÂY LÀ HỢP CHẤT
Đúng 0
Bình luận (0)
đốt cháy hết một lượng lưu huỳnh (S) cháy trong 2,24 lít khí oxi (ở đktc) sinh ra khí sunfurơ (SO2). Hãy cho biết :a, thể tích khí sunfurơ thu được ở đktc ?b, khối lượng lưu huỳnh đã bị đốt cháy ?
S + O2 →SO2
a) nO2 = 2,24/22,4 = 0,1 mol
=> nSO2 = 0,1 mol
<=> V SO2 = 0,1 .22,4 = 2,24 lít
b) nS = O2 = 0,1 mol
=> mS = 0,1.32 = 3,2 gam
Đúng 0
Bình luận (0)
S + O2 →SO2
a) nO2 = 2,24/22,4 = 0,1 mol
=> nSO2 = 0,1 mol
<=> V SO2 = 0,1 .22,4 = 2,24 lít
b) nS = O2 = 0,1 mol
=> mS = 0,1.32 = 3,2 gam
Đúng 0
Bình luận (0)
bài 3 Lưu Huỳnh cháy trong không khí tạo ra khí sunfurơleft(SO_2right) Đây là một chất khí độc có mùi hắc gây hovaf là một trong các khí gây ra hiện tượng mưa ãita)Viết phương trình hóa học của phản ứng b)Tính thể khí left(SO_2right) tạo ra và thể tích không khí cần dùng cho đốt cháy hết 3,2 gam lưu huỳnh (biết các thể tích khí đo ở dktc: trong không khí õi chiếm 20%về thể tích )
Đọc tiếp
bài 3 Lưu Huỳnh cháy trong không khí tạo ra khí sunfurơ\(\left(SO_2\right)\) Đây là một chất khí độc có mùi hắc gây hovaf là một trong các khí gây ra hiện tượng mưa ãit
a)Viết phương trình hóa học của phản ứng
b)Tính thể khí \(\left(SO_2\right)\) tạo ra và thể tích không khí cần dùng cho đốt cháy hết 3,2 gam lưu huỳnh (biết các thể tích khí đo ở dktc: trong không khí õi chiếm 20%về thể tích )
a) Phương trình phản ứng hóa học :
S + O2 \(\rightarrow\) SO2
b) Số mol lưu huỳnh tham gia p.ứng là :
nS = 3,2/32 = 0,1 (mol)
Theo phương trình ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VSO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% thể tích của không khí nên thể tích không khí cần là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
Đúng 0
Bình luận (0)
a)Phương trình phản ứng hóa học :
\(S+O_2->SO_2\)
b)Số mol lưu huỳnh thangia phản ứng
\(n_s\) =\(\frac{3,2}{32}\) =0,1(mol)
theo phương trình ta có
\(n_{so2}=n_s=n_{o2}\)
Thể tích khí sunfurơ sing ra được ở dktc là
\(V_{o2}=22,4.0,1=2,24\left(l\right)\)
tương tự thể tích khí cần dùng ở dktc là
\(V_{o2}=22,4.0,1=2,24\left(l\right)\)
Vì khí õi chiếm 20% về thể tích của không khí veentheer tích không khí cầ dùng là
\(V_{kk}=5.v_{o2}=5.2,24=11,2\left(l\right)\)
Chúc bạn học tốt ![]()
![]()
Đúng 0
Bình luận (0)
a)
S + O2 --> SO2
b)
nS=\(\frac{3,2}{32}=0,1\left(mol\right)\)
nO2=nS=nSO2=0,1(mol)
VO2=VSO2(đktc)=0,1.22,4=2,24(lít)
thể tích không khí cần để đốt cháy 3,2 gam lưu huỳnh là:
\(\frac{2.24}{20}.100=11,2\)(lít)
Đúng 0
Bình luận (0)
Giúp mình bài này nha, đây là hóa học nhưng vì ko biết làm mà lại cần gấp nên mình mới hỏiĐề: Lưu huỳnh (S) cháy trong không khí sinh ra khí sunfurơ (SO2). Biết lưu huỳnh cháy là tác dụng với oxi trong không khí.a. Viết phương trình hóa họcb, Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1,5 mol nguyên tử lưu huỳnh.Chú ý câu b, ko cần giải câu a cũng được nhé ~♥Thanh you♥~
Đọc tiếp
Giúp mình bài này nha, đây là hóa học nhưng vì ko biết làm mà lại cần gấp nên mình mới hỏi
Đề: Lưu huỳnh (S) cháy trong không khí sinh ra khí sunfurơ (SO2). Biết lưu huỳnh cháy là tác dụng với oxi trong không khí.
a. Viết phương trình hóa học
b, Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 1,5 mol nguyên tử lưu huỳnh.
Chú ý câu b, ko cần giải câu a cũng được nhé ~♥Thanh you♥~
a) Phương trình phản ứng hóa học :
S + O2 →→ SO2
b) Số mol lưu huỳnh tham gia phản ứng :
nS=3,232=0,1(mol)nS=3,232=0,1(mol)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% về thể tích của không khí nên thể tích không khí cần dùng là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)
Đúng 0
Bình luận (0)



















